A. Tinjauan Umum
Fermentasi merupakan proses mikrobiologi
yang dikendalikan oleh manusia untuk memperoleh produk yang berguna, dimana
terjadi pemecahan karbohidrat dan asam amino secara anaerob. Peruraian dari kompleks menjadi sederhana
dengan bantuan mikroorganisme sehingga menghasilkan energi. (Perry, 1999)
Industri
fermentasi di negara-negara maju sudah berkembang sedemikian pesatnya, termasuk
dalam produksi hasil-hasil pemecahan atau metabolit primer oleh mikroba (asam,
asam amino, alkohol), hasil metabolit sekunder (antibiotik, toksin), produksi
masa sel (protein sel tunggal), enzim, dan sebagainya. Mikroba yang umum
digunakan dalam industri fermentasi termasuk dalam bakteri dan fungi tingkat
rendah yaitu kapang dan khamir.
Berdasarkan Silcox dan Lee, proses fermentasi yang baik adalah:
1. Mikroorganisme dapat membentuk produk yang
diinginkan
2. Organisme ini harus berpropagasi secara
cepat dan dapat mempertahankan
keseragaman biologis, sehingga
memberikan yield yang dapat diprediksi.
3.
Raw material sebagai substrat
ekonomis
4.
Yieldnya dapat diterima
5.
Fermentasi cepat
6. Produk mudah diambil dan dimurnikan
Asam asetat
memiliki beberapa nama antara lain asam etanoat, vinegar (mengandung minimal 4
gram asam asetat per 100 larutan), atau asam cuka. Asam asetat merupakan
senyawa organik yang mengandung gugus asam karboksilat. Rumus molekul dari asam
asetat adalah C2H4O2. Rumus
ini seringkali ditulis dalam bentuk CH3-COOH, CH3COOH,
atau CH3CO2H. Asam asetat memiliki sifat antara lain (Perry, 1999):
Ø Berat molekul 60,05
Ø berupa cairan jernih (tidak berwarna)
Ø berbau khas
Ø mudah larut dalam air, alkohol, dan eter
Ø larutan asam asetat dalam air merupakan
sebuah asam lemah
(korosif)
Ø mempunyai titik didih 118,1 oC
Ø mempunyai titik beku 16,7 oC
Ø Spesific grafity 1,049
B. Proses Produksi
Ø Produksi asam asetat dengan cara :
a.
Fermentasi Aerob
H12O6 → 2 C2H5OH → 2 CH3COOH
+ H2O + 116 kal
glukosa etanol cuka
asam cuka
b. Fermentasi Anaerob
|
|
Clostridium thermoaceticum
|
|
C6H12O6 → CH3COOH
+ Q
glukosa cuka asam cuka
c. Sintetis
·
Karbonilasi methanol
·
Oksidasi
asetaldehida
Pembahasan ditekankan pada
produksi asam asetat dengan cara fermentasi aerob dan fermentasi anaerob.
Ø Bahan Baku dalam proses fermentasi pembuatan asam asetat :
-
Buah-buahan, kentang,
biji-bijian, bahan yang mengandung cukup banyak gula, atau alkohol
-
Bakteri asetat (Bacterium aceti) yaitu Acetobacter
untuk proses aerob dan bakteri dari genus Clostridium
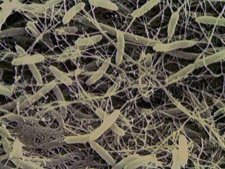
Gambar 1. Acetobacter aceti
Ø Proses fermentasi pembuatan asam
asetat atau vinegar :
A).
Fermentasi secara Aerob
a. Metoda lambat (Slow Methods)
-
Biasanya untuk bahan baku berupa
buah-buahan
-
Etanol tidak banyak bergerak
atau mengalir karena proses dilakukan pada suatu tangki batch
-
Memasukan
jus buah, yeast, dan bakteri vinegar ke dalam
tangki
-
Sebagian
jus buah terfermentasi menjadi etanol (11-13 % alkohol) setelah beberapa hari
-
Fermentasi
etanol menjadi asam asetat terjadi pada permukaan tangki
-
Bakteri
vinegar di permukaan larutan yang membentuk lapisan agar-agar tipis mengubah
etanol menjadi asam asetat atau vinegar (asetifikasi)
-
Proses
ini memerlukan temperatur 21- 29 oC
-
Jatuhnya
lapisan tipis agar-agar dari bakteri vinegar akan memperlambat asetifikasi. Permasalahan
ini bisa dicegah dengan memasang lapisan yang dapat mengapungkan lapisan tipis
agar-agar dari bakteri vinegar
-
Kelebihan Metoda lambat (Slow Methods) :
a)
Proses sangat sederhana
-
Kekuranagan Metoda lambat (Slow Methods) :
a) Proses relative lama berminggu-minggu atau
berbulan-bulan
b) Jatuhnya lapisan tipis agar-agar dari
bakteri vinegar akan memperlambat asetifikasi
b. Metoda cepat (Quick Methods)
atau German
process
-
Biasanya
untuk bahan baku berupa etanol cair
-
Bahan
baku untuk basis 1 ton asam asetat(100%) :
·
Alkohol(95
%) sebanyak 1.950 lb
·
Sedikit
nutrisi
·
Udara
sebanyak 11.000 lb
-
Etanol
mengalami perpindahan selama proses
-
Proses
fermentasi terjadi di dalam tangki pembentukan (Frings generator) yang terbuat dari kayu atau besi.
-
Bagian-bagian
dari tangki pembentukan :
a) Bagian atas, tempat alkohol dimasukkan
b) Bagian tengah, terdapat bahan isian (berupa:
kayu, tongkol jagung, rottan) di bagian ini untuk memperluas bidang kontak
rektan (etanol dan oksigen). Bahan isian mula-mula disiram dengan larutan
vinegar yang mengandung bakteri asetat sehingga dipermukaan bahan isian akan
tumbuh bakteri asetat.
c) Bgian bawah, digunakan sebagai tempat
mengumpulkan produk vinegar.
-
Mendistribusikan
campuran etanol cair (10,5 %), vinegar(1 %), dan nutrisi melalui bagian atas tangki dengan alat sparger
-
Campuran
mengalir turun melalui bahan isian dengan sangat lambat
-
Udara
dialirkan secara countercurrent melalui
bagian bawah tangki
-
Panas
yang timbul akibat reaksi oksidasi diambil dengan pendingin. Pendingin dipasang
pada aliran recycle cairan
campuran(yang mengandung vinegar,etanol, dan air) dari bagian bawah tangki. Temperatur
operasi dipertahankan pada rentang suhu 30-35 oC
-
Produk
yang terkumpuk di bagian bawah tangki mengandung asam asetat optimum sebesar 10-
10,5 %. Sebagian produk direcycle dan
sebagian yang lain di keluarkan dari tangki
-
Bakteri
asetat akan berhenti memproduksi asam asetat jika kadar asam asetat telah
mencapai 12-14 %
-
Bahan
baku 2.500 gal dengan produk 10,5 % asam asetat memerlukan waktu proses 8-10
hari
-
Kelebihan
Metoda cepat (Quick
Methods) atau German process :
a) Biaya proses rendah, relatif sederhana dan
kemudahan dalam mengontrol
b) Konsentrasi produk asam asetat besar
c) Tangki proses membutuhkan sedikit tempat
peletakannya
d) Penguapan sedikit
-
Kekurangan
Metoda cepat (Quick Methods) atau German process :
a) Waktu tinggal terlalu lama bila
dibandingkan Metoda Perendaman (Submerged
Method)
b) Pembersihan tangki cukup sulit
Gambar 2.
Frings Generator
c. Metoda Perendaman (Submerged Method)
-
Umpan
yang mengandung 8-12 % etanol diinokulasi dengan Acetobacter acetigenum
-
Temperatur
proses dipertahankan pada rentang suhu 24-29 oC
-
Bakteri
tumbuh di dalam suspensi antara gelembung udara dan cairan yang difermentasi
-
Umpan
di masukan melewati bagian atas tangki
-
Udara
didistribusikan dalam cairan yang difermentasi sehingga membentuk gelembung-
gelembung gas. Udara keluar tangki melewati pipa pengeluaran di bagian atas
tangki
-
Temperatur
proses dipertahankan dengan menggunakan koil pendingin stainless steel yang terpasang di dalam tangki
-
Defoamer yang terpasang di bagian atas tangki membersihkan
busa yang terbentuk dengan sistem mekanik
-
Kelebihan Metoda Perendaman (Submerged
Method):
a) Hampir disemua bagian tangki terjadi
fermentasi
b) Kontak antar reaktan dan bakteri semakin
besar
-
Kekurangan Metoda Perendaman (Submerged Method):
a) Biaya operasi relatif mahal
B).
Fermentasi secara Anaerob
-
Menggunakan
bakteri Clostridium thermoaceticum
-
Mampu
mengubah gula menjadi asam asetat
-
Temperatur
proses sekitar 45- 65 oC; pH 2-5
-
Memerlukan
nutrisi yang mengandung karbon, nitrogen dan senyawa anorganik
-
Kelebihan
proses anaerob :
a) Mengubah gula menjadi sama asetat dengan
satu langkah
b) Bakteri tumbuh dengan baik pada temperatur
60 oC. Perbedaan temperatur yang besar antara suhu media dengan suhu
air pendingin memudahkan dalam pembuangan panas
c) Kontaminasi dengan organisme yang
membutuhkan bisa diminimalisasi karena bekerja pada kondisi anaerob
d) Organisme yang hanya dapat hidup dalam
kondisi mendekati pH netral akan mati karena operasi fermentasi dilakukan pada
kondisi asam pH 4,5
-
Kekurangan
proses anaerob :
a) Kosentarasi asam asetat lebih rendah
dibandingkan dengan proses aerob
b) Biaya proses lebih mahal dibandingkan
dengan proses aerob
Ø Pemurnian
Distilasi/penyulingan
Dari
distilasi bertingkat akan dihasilkan beberapa jenis asam asetat :
Ø Asam asetat glacial (99,5 %)
Ø Asam asetat teknis (80 %)
Secara
komersial kadar asam asetat sebesar 6, 28, 30, 36, 60, 70, dan 80 %
C.
Manfaat dan Penggunaan Produk
Beberapa Kegunaan asam asetat
atau vinegar adalah sebagai berikut :
2. Pengatur keasaman
pada industri makanan
4. Minuman fungsional misal: cuka apel
5. Sebagai bahan baku untuk pembuatan bahan
kimia lain :
-
Vinil
asetat
-
Selulosa
asetat
-
Asetat
Anhidrit
-
Ester
Asetat
-
Garam Asetat
Referensi :
Frazier. Food Microbiology.
1978. McGraw-Hill. Amerika
Keyes, Keyes. Industrial
Chemicals. 1950. McGraw-Hill. Amerika
Perry. Perry’s Chemical
Engineers’ Handbook. 1999. McGraw-Hill. Amerika
www.wikipedia.com